α,β -不饱和羰基化合物因其选择性加氢产物是一种重要的有机中间体而具有较高的经济价值,在香料、医药、农业等领域应用广泛。α,β -不饱和羰基化合物中C=C和C=O双键同时存在,加氢后产物复杂,因此研究α,β -不饱和羰基化合物C=O双键选择性加氢具有重要意义。贵金属催化剂常用于α,β -不饱和羰基化合物选择性加氢反应中,Au、Ru、Pt、Pd等贵金属对该反应都具有良好的催化效果[1-3]。相比较而言,Pd金属催化剂则更有利于C=C双键加氢,而Pt金属催化剂更有利于C=O双键加氢[4-5]。由于贵金属催化剂存在价格高、不适合大规模工业化生产等缺点,因此低成本的非贵金属催化剂被广泛开发应用。非贵金属Co、Ni、Cu等也常用于不饱和羰基化合物的催化加氢中。Ni基催化剂主要用于C=C双键加氢,Mahata等[6]将碳沉积到活性组分Ni上得到Ni/C催化剂,发现在巴豆醛和异佛尔酮的加氢反应中,Ni/C催化剂对C=C双键有较高的加氢选择性。Prakash等[7]以葡萄糖作为还原剂制备了Ni-Cu/TiO2、Ni-Au/TiO2、Ni-Ag/TiO2等双金属催化剂,发现在低温条件下,Ni-Au双金属催化剂展现出较高的肉桂醛转化率,并且肉桂醇选择性为47.4%。Co和Cu均是较好的C=O双键加氢催化剂,Joseph等[8]通过浸渍法将Co负载在TiO2、SiO2和Al2O3上,将这些催化剂用于液相催化肉桂醛加氢反应上,发现由TiO2负载的Co基催化剂在120 ℃、1 MPa压力下转化率和选择性最好,肉桂醇的选择性达到了58%。通过共沉淀法制备Cu/MgO、Cu/SiO2和Cu/ZnO催化剂[9],将其用来进行糠醛选择性加氢反应,在适宜的反应条件下,糠醇的收率分别为96%、73%和94%。
顺酐是重要α,β -不饱和羰基化合物之一,其选择性加氢得到的丁二酸酐(succinic anhydride, SA)、γ-丁内酯(γ-butyrolactone,GBL)等产物,是具有较高附加值的化学品[10-11]。Meyer等[12]考察了不同Ni负载量的Ni/SiO2-Al2O3对顺酐催化加氢催化效果,表明低Ni负载量的Ni/SiO2-Al2O3催化剂催化顺酐加氢反应的主要产物为SA,而当Ni负载量达到10%时,主要产物为GBL。赵永祥等[13]将Ni负载在SiO2、Al2O3和Al2O3-SiO2三种载体上,三种催化剂的顺酐转化率均能达到99%以上,但其对产物的选择性不同,Ni/SiO2催化剂主要产物是GBL,其选择性为80.1%,而Ni/ Al2O3催化剂的主要产物则是SA,其选择性可达95.22%。夏晓丽等[14]通过在页硅酸镍中引入助剂Mo,在温度160 ℃和压力5 MPa的反应条件下,引入Mo质量分数为3%的页硅酸镍催化剂顺酐转化率能达到100%,GBL的选择性为27%。Cu-Zn-Cr表现出较高顺酐加氢活性和GBL选择性,但Cr元素具有较强的毒性会导致环境污染和人类身体健康。邱爱玲等[15]通过沉淀法制备的Cu-CeO2-Al2O3在常压气相加氢中表现出优良的催化效果,转化率和GBL选择性均达到了100%,但催化剂容易失活。
国内外大量研究表明,Ni基催化剂主要用于C=C双键加氢,而Cu基催化剂则主要用于C=O双键加氢,但对Ni-Cu双金属催化剂选择性加氢C=C、C=O双键的研究较少。本研究采用蒸氨法制备一系列Ni-Cu/SiO2催化剂,通过XRD、BET、XPS、H2-TPD、H2-TPR等表征方法,研究了Ni、Cu双金属的比例在顺酐常压气相选择性加氢反应中对产物SA和GBL选择性的调控规律,并筛选了适用于顺酐加氢制备GBL联产SA的催化剂进行反应条件优化。
1 试验部分1.1 催化剂制备采用蒸氨法制备xNiyCu/SiO2系列催化剂,其中x为Ni的质量分数,y为Cu的质量分数。以20Ni20Cu/SiO2为例,根据各20%的Cu、Ni的负载量计算出所需硝酸镍和硝酸铜的质量,称取适量Ni(NO3)2·6H2O和Cu(NO3)2·3H2O加入去离子水中,搅拌至完全溶解,再加入计算出的NH3·H2O搅拌,直至底部沉淀完全溶解,形成金属-氨络合物络合物溶液; 然后向溶液中缓慢滴加碱性硅溶胶,室温下密闭搅拌4 h,在100 ℃下蒸氨至溶液pH=7。前驱物进行抽滤,洗涤三次,滤饼置于120 ℃烘箱干燥后于500 ℃空气下焙烧4 h,得到催化剂粉末,压片、破碎,选取20~40目颗粒备用。其余催化剂除Ni、Cu质量分数不同外,制备步骤同上。
1.2 催化剂表征采用日本理学公司Rigaku UtimaⅣ型X-射线衍射仪(XRD)对催化剂进行物相分析。扫描速率为5 °/min,扫描范围为2θ=5°~80°。采用日本麦奇克拜耳(Microtrac BELSORP-mini Ⅱ)全自动物理吸附仪对催化剂进行比表面、孔体积及孔径分布分析。采用日立SU1510扫描电镜(SEM)对催化剂进行形貌分析。采用赛默飞Thermo Scientific ESCALAB 250Xi X-射线光电子能谱仪(XPS)对催化剂进行元素价态分析。采用日本麦奇克拜尔公司BELCAT-B3化学吸附仪对催化剂进行H2程序升温脱附(H2-TPD)和程序升温还原(H2-TPR)分析。
1.3 催化剂性能评价顺酐气相加氢在常压固定床反应装置中进行,将一定量催化剂装入反应管中部,催化剂上下两端以石英棉固定。反应前催化剂用纯H2原位还原8 h,然后采用微量注射器将原料液送入反应管中,在一定条件下进行反应,所得产物用冷阱收集。使用气相色谱(岛津GC-2014,色谱柱DB-624)对产物进行离线分析。顺酐转化率及产物选择性计算公式分别如下:

式(1)~(2)中:Fin、Fout和Pi,out分别表示为顺酐进料摩尔浓度、顺酐反应后摩尔浓度和产物i的摩尔浓度。
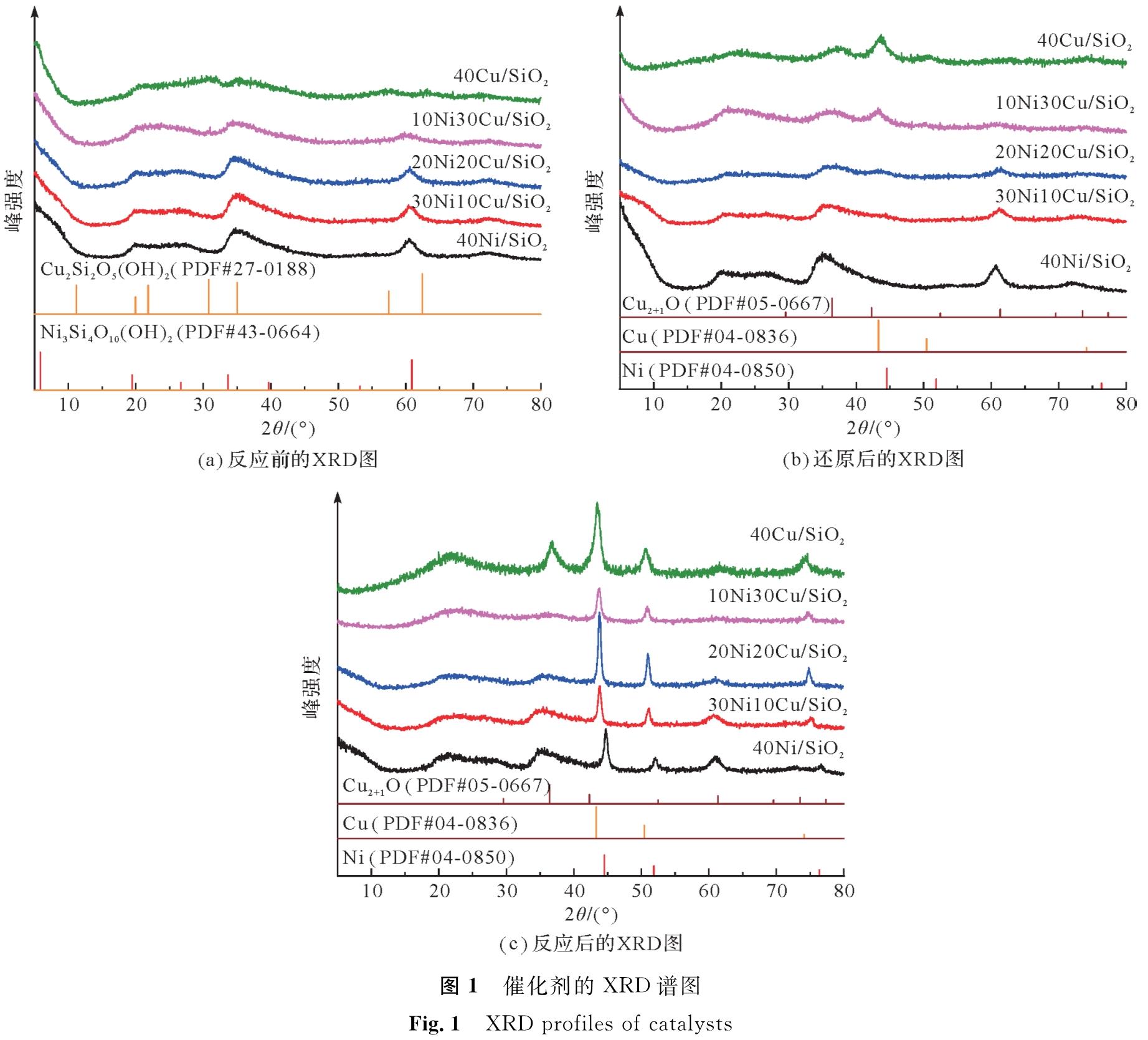
2 结果与讨论2.1 催化剂物相分析催化剂的XRD谱图见图1。图1(a)为催化剂反应前的XRD图谱。图1(a)表明在2θ为33.7°和60.9°处有明显的页硅酸镍(PDF#43-0664)的特征峰,在30.8°、35.0°、57.5°和62.4°处为页硅酸铜(PDF#27-0188)的特征峰。页硅酸铜的特征峰比页硅酸镍的特征峰弱,表明页硅酸铜颗粒的粒径比页硅酸镍颗粒的粒径小。还原后的催化剂XRD谱图(图1(b))中,在33.7°和60.9°处仍存在明显的页硅酸镍的特征峰,表明页硅酸镍结构稳定,不易被还原。在43.3°、50.4°和74.1°处呈现为Cu的特征峰; 在2θ为36.4°和61.3°处呈现为Cu2+1O(PDF#05-0667)的特征峰,说明页硅酸铜较页硅酸镍更容易被还原; 还原后的催化剂Cu0和Cu+是催化剂的活性中心。反应后催化剂的XRD谱图见图1(c),反应后的40Cu/SiO2催化剂在43.3°、50.4°和74.1°处呈现为Cu(PDF#04-0836)的特征峰,在36.4°和61.3°处呈现为Cu+的特征峰,在44.5°、51.8°和76.4°处呈现为Ni(PDF#04-0850)的特征峰。其余3种Ni-Cu/SiO2催化剂在 Ni(44.5°)和Cu(43.3°)特征峰之间出现了一个特征峰,其随Cu含量的增加,向低峰值的位置移动,Cu会使Ni产生缺陷位点,从而形成Ni-Cu合金或金属间混合物[16]。反应后的40Ni/SiO2催化剂中在33.7°和60.9°处仍存在页硅酸镍的特征峰,表明了页硅酸镍具有稳定的结构。
2.2 催化剂形貌分析
催化剂SEM图(图2)表明40Cu/SiO2催化剂表面由疏松的不规则的片状物质组成,分布均匀,该结构应为层状页硅酸铜的结构。而40Ni/SiO2催化剂的表面也由片状物质组成,该结构应为层状页硅酸镍的结构,其他3种Ni-Cu/SiO2催化剂也都出现了层状页硅酸盐的结构和小部分颗粒积聚的现象。
图2 不同Ni-Cu/SiO2催化剂的SEM图
Fig.2 SEM images of different Ni-Cu/SiO2 catalysts
2.3 催化剂孔结构分析
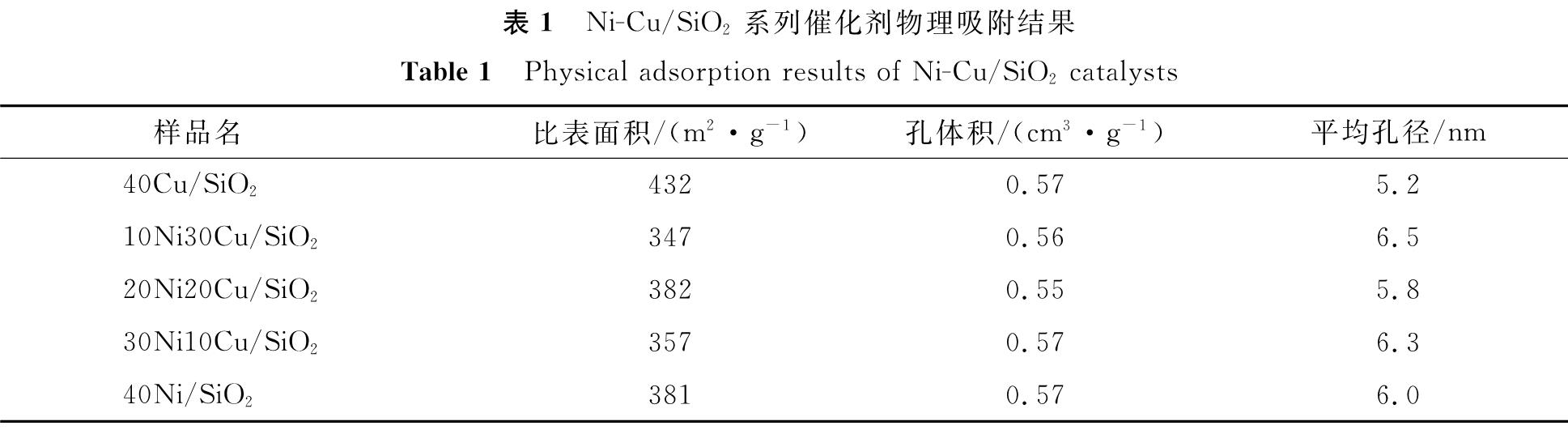
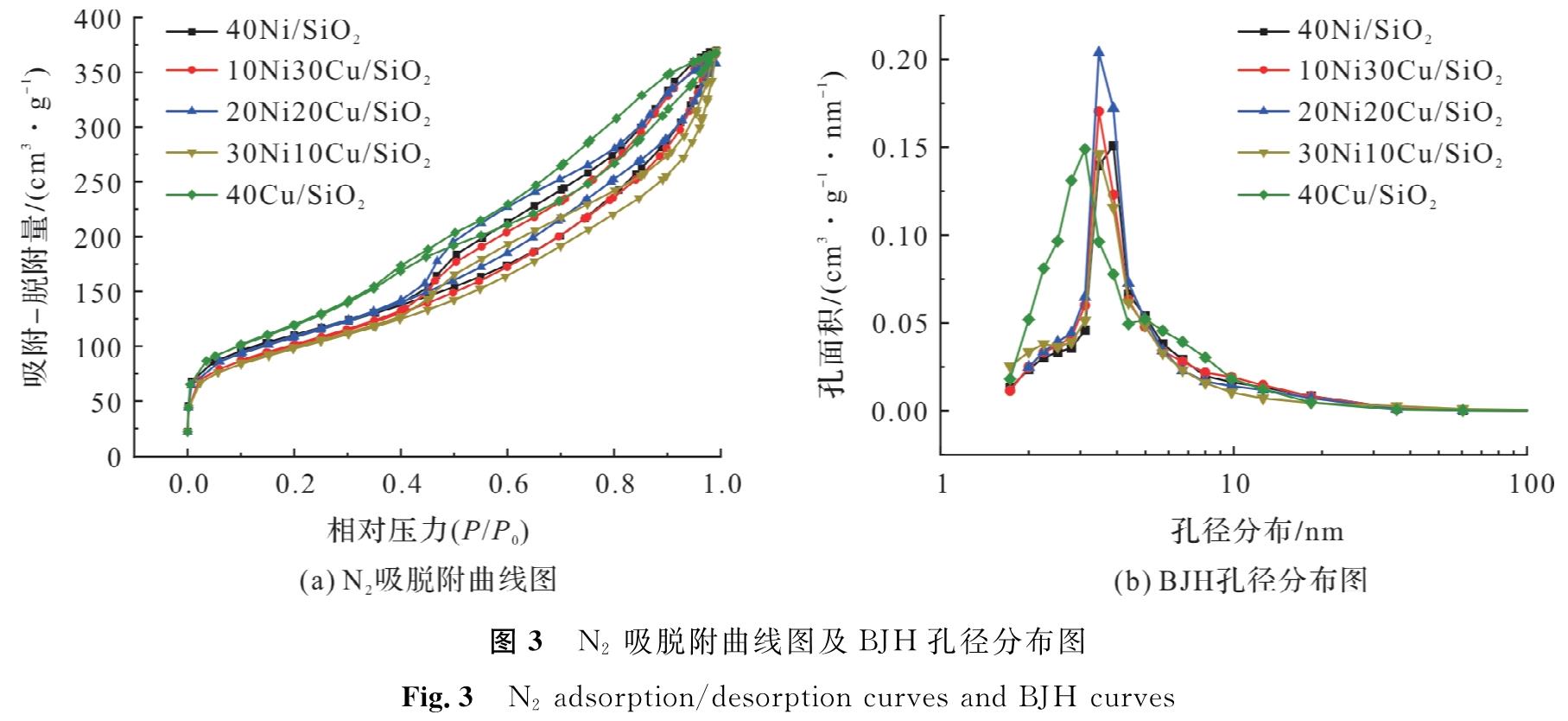
Ni-Cu/SiO2系列催化剂物理吸附结果见表1。由表1可知,40Cu/SiO2的比表面积最大,这是由于该催化剂的平均孔径最小,孔道较多,催化剂与反应物的接触面积增大,增强了对氢气的吸附能力,更有利于加氢反应的进行。随着Ni的加入,催化剂的比表面积减小,平均孔径增大,该现象是Ni-Cu双金属协同作用的结果。从不同Ni-Cu/SiO2催化剂的N2吸脱附曲线图(图3a)可以看出,Ni-Cu/SiO2系列催化剂的N2吸脱附等温线均具有明显的滞留回环,是典型的Ⅳ型吸脱附等温线,表明Ni-Cu/SiO2系列催化剂均为介孔结构。由BJH(Barret-Joyner-Halenda)孔径分布图(图3b)可以看出,Ni-Cu/SiO2系列催化剂的孔径均主要分布在2~10 nm之间,且催化剂的孔径比较均一。
表1 Ni-Cu/SiO2系列催化剂物理吸附结果
Table 1 Physical adsorption results of Ni-Cu/SiO2 catalysts
图3 N2吸脱附曲线图及BJH孔径分布图
Fig.3 N2 adsorption/desorption curves and BJH curves
2.4 催化剂元素价态分析
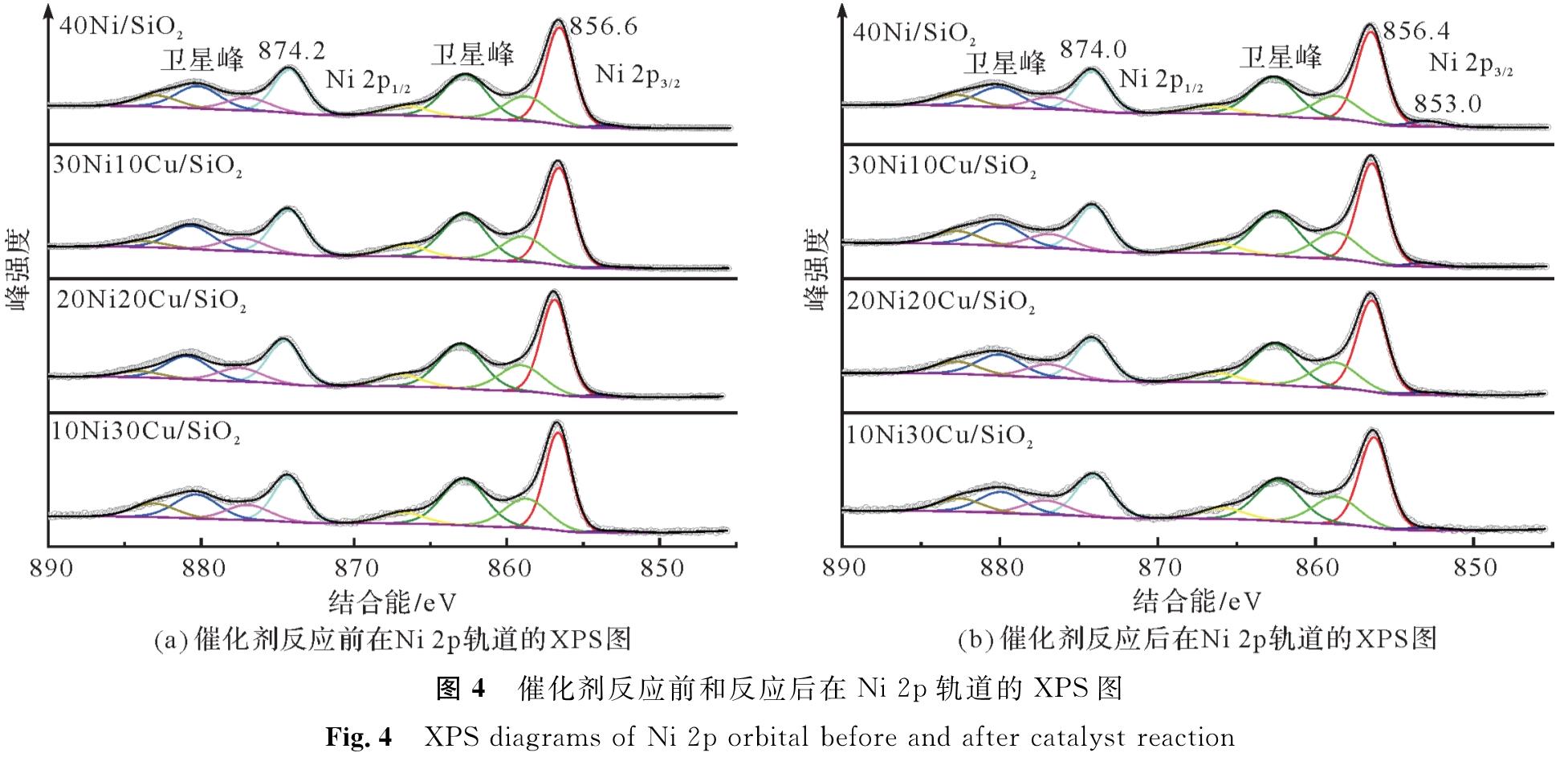
图4为Ni-Cu/SiO2催化剂反应前和反应后在Ni 2p轨道的XPS图。对于反应前的催化剂,它在856.6、874.2 eV结合能附近的峰为Ni2+,在862.0、880.0 eV结合能附近为Ni2+的卫星峰,Ni2+主要来源于页硅酸镍。页硅酸镍中的镍与载体SiO2产生的强相互作用,导致页硅酸盐中Ni2+的结合能比传统硅负载镍中Ni2+的结合能偏高[17]。反应后的催化剂在856.4、874.0 eV结合能附近的峰为Ni2+,说明反应后的催化剂中仍存在页硅酸镍结构。853.0 eV结合能附近的峰归属为Ni0,Ni0来源于少量被还原的页硅酸镍,由于页硅酸镍的结构稳定,所以只有少量的Ni被还原。这与反应后催化剂的XRD结果一致。
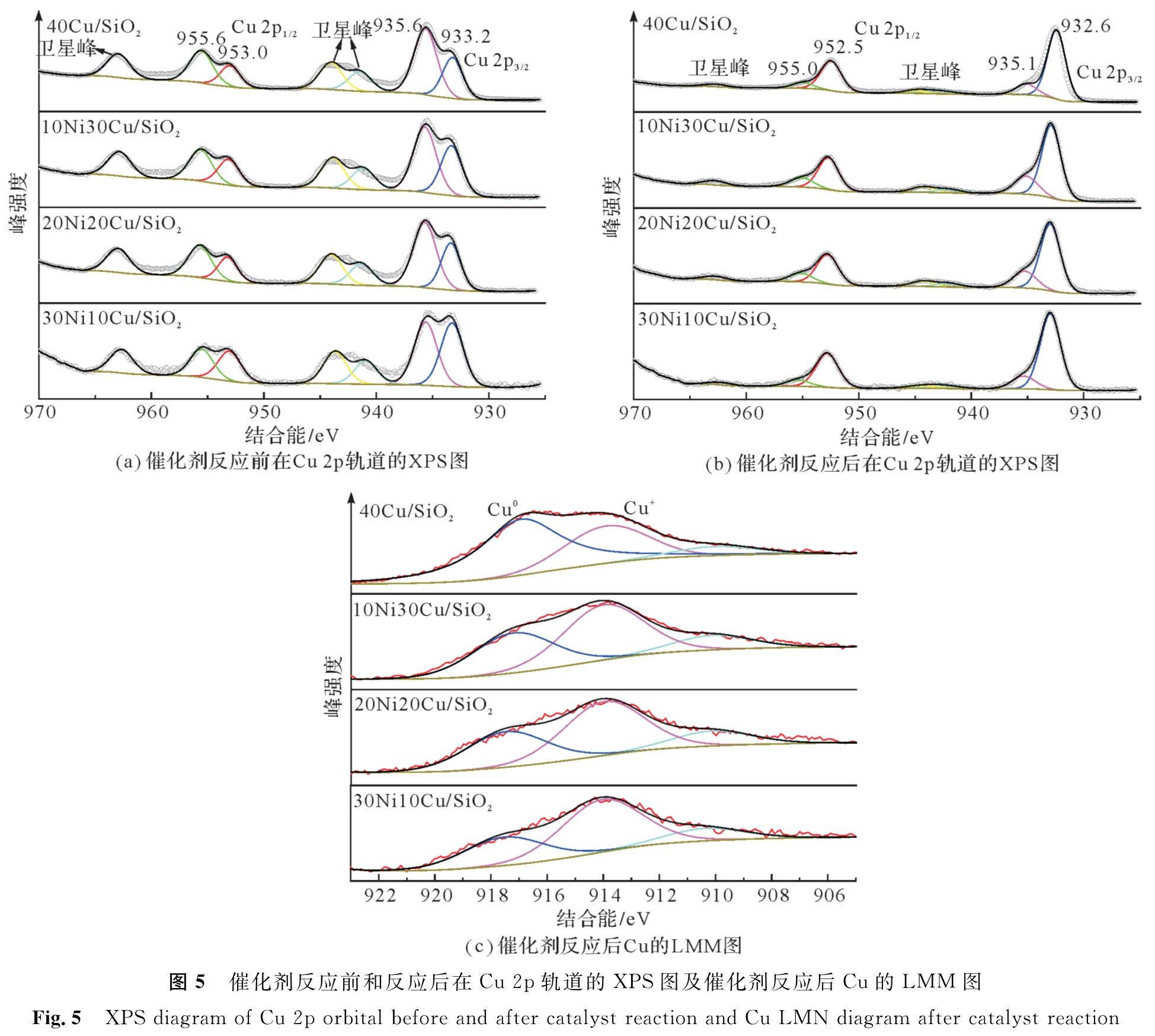
催化剂反应前和反应后在Cu 2p轨道的XPS图及催化剂反应后Cu LMM图见图5。反应前催化剂在933.2、935.6 eV结合能附近的峰分别为氧化铜和页硅酸铜中Cu2+的2p3/2轨道的特征峰[18],953.0、955.6 eV结合能附近的峰分别为氧化铜和页硅酸铜中Cu2+的2p1/2轨道的特征峰。由此可见,反应前的催化剂主要以页硅酸铜的形式存在。在941.4、944.0、962.9 eV结合能附近的峰为Cu2+的卫星峰[19]。反应后的催化剂中在932.6、952.5 eV附近的峰归属为Cu+/Cu0的2p3/2轨道和2p1/2轨道,Cu+/Cu0的峰随着镍的加入向结合能高的方向移动,Cu结合能的增加是由于Cu与Ni之间的协同作用使得电子由Cu向Ni转移引起[20]。而Cu2+所属的峰及其卫星峰强度减弱,可见反应后的催化剂表面主要以Cu+/Cu0的形式存在。通过Cu LMM谱图进一步确定铜基催化剂表面物种。在913.9、918.0 eV[21]结合能附近的峰分别对应Cu+和Cu0,表明Cu0和Cu+在反应后的催化剂表面是共存的,说明经还原后的催化剂的主要活性中心是Cu0和Cu+。这与XRD结果中出现Cu0和Cu+衍射峰一致。
图5 催化剂反应前和反应后在Cu 2p轨道的XPS图及催化剂反应后Cu的LMM图
Fig.5 XPS diagram of Cu 2p orbital before and after catalyst reaction and Cu LMN diagram after catalyst reaction
2.5 H2-TPD分析
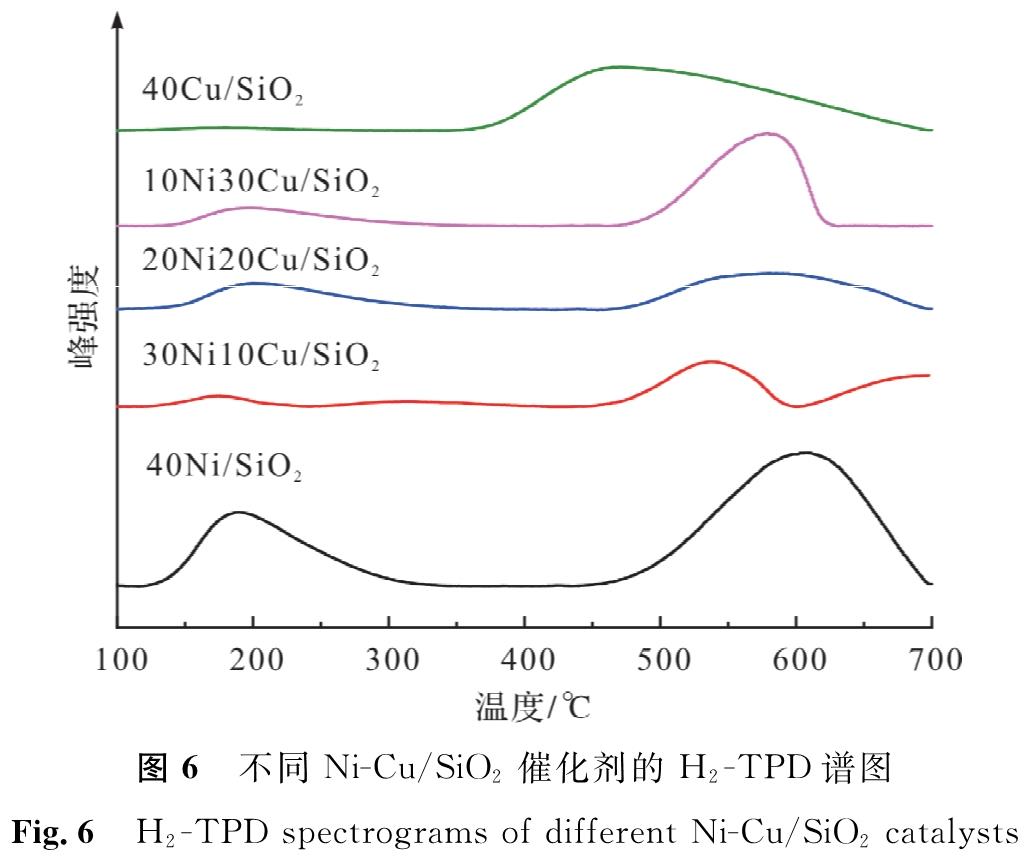
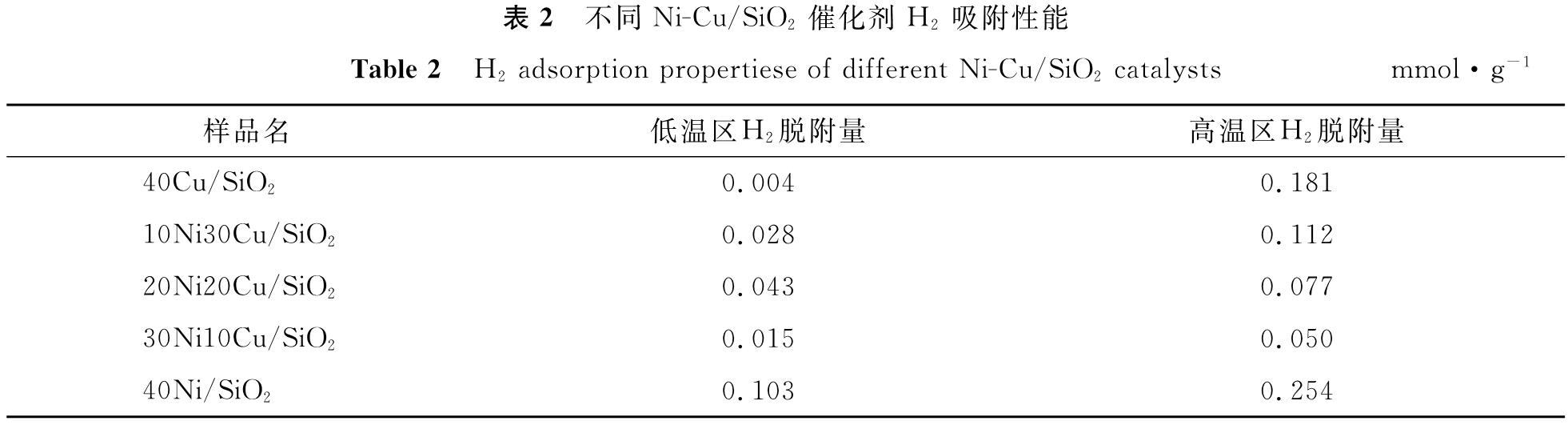
H2的化学吸附是发生催化加氢反应的重要前提。对比40Ni/SiO2和40Cu/SiO2催化剂,其脱附峰的位置和峰面积均发生了变化,说明Ni-Cu双金属的协同作用对H2的吸附产生了一定的影响。不同Ni-Cu/SiO2催化剂的H2-TPD谱图见图6,不同Ni-Cu/SiO2催化剂H2吸附性能见表2。图6和表2表明所有Ni-Cu/SiO2催化剂都具有较高的H2吸附强度和吸附量,这说明催化剂具有较好的加氢性能。含镍催化剂在低温(130~300 ℃)和高温(450~700 ℃)出现了两个脱附峰,低温脱附峰归属于Ni的活性位点的吸附,表明Ni是较好的低温加氢催化剂。而高温脱附峰归属于催化剂表面氢裂解。含铜催化剂在高温(400~700 ℃)出现了明显的脱附峰,源于催化剂表面的氢裂解[22]。
图6 不同Ni-Cu/SiO2催化剂的H2-TPD谱图
Fig.6 H2-TPD spectrograms of different Ni-Cu/SiO2 catalysts
表2 不同Ni-Cu/SiO2催化剂H2吸附性能
Table 2 H2 adsorption propertiese of different Ni-Cu/SiO2 catalystsmmol·g-1
2.6 H2-TPR分析
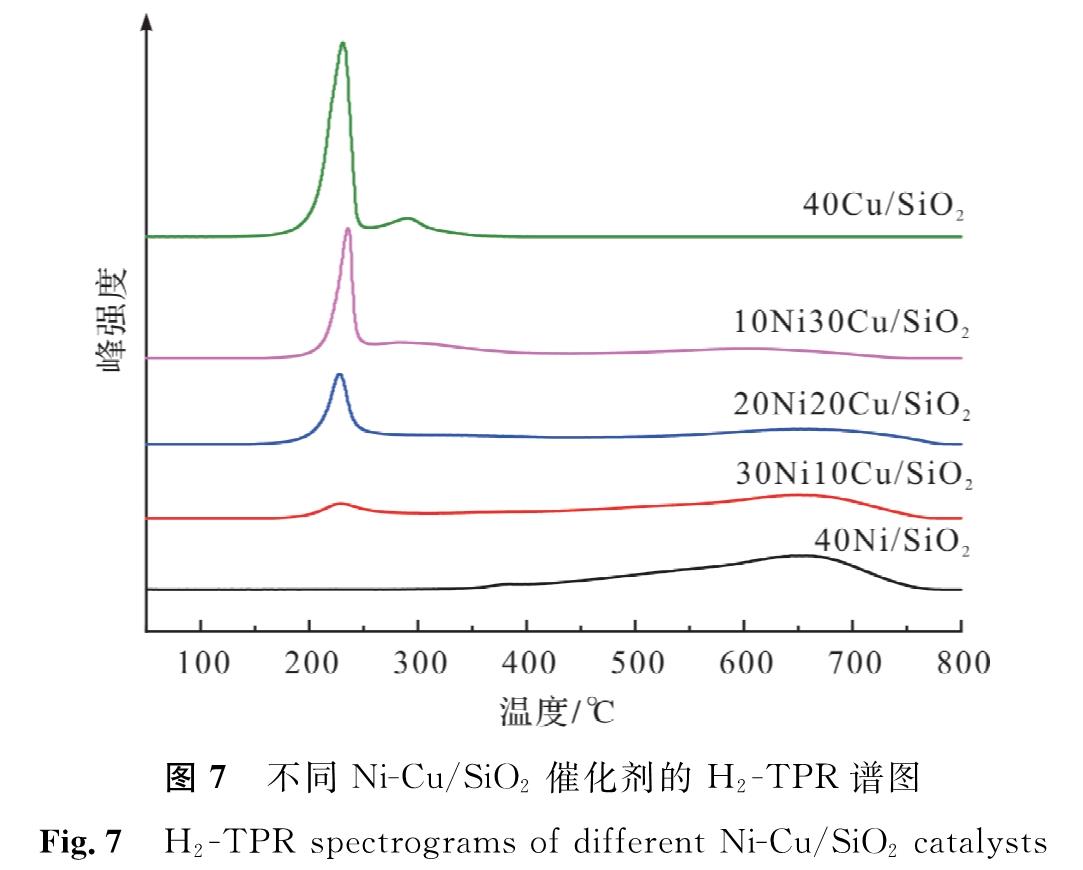
图7为不同Ni-Cu/SiO2催化剂的H2-TPR谱图。由图7可知,40Cu/SiO2在230 ℃附近出现尖锐的还原峰,归属于页硅酸铜中高度分散的Cu2+物种还原,290 ℃附近出现的肩峰归属于粒径较大的CuO物种还原。40Ni/SiO2催化剂在665 ℃附近出现了宽泛的还原峰,归属于页硅酸镍的还原。宽泛还原峰是由页硅酸镍中镍与载体SiO2间的强相互作用造成[23]。而Ni-Cu双金属催化剂中出现了的两个还原峰,在230 ℃附近的还原峰属于页硅酸铜的还原,在665 ℃附近的高温还原峰属于页硅酸镍的还原; 与Cu、Ni单金属催化剂的还原峰相比,Ni-Cu双金属具有协同作用使得两个还原峰与单金属的还原峰相比有所偏移。40Ni/SiO2催化剂中Ni2+的还原峰中心温度处于630~665 ℃之间说明页硅酸镍中的Ni2+在500 ℃的还原条件下难以被还原,这与XRD、XPS中出现的结果是一致的。Ni-Cu双金属催化剂中的两个还原峰的峰面积随着Ni、Cu含量的变化表现出规律性变化。
图7 不同Ni-Cu/SiO2催化剂的H2-TPR谱图
Fig.7 H2-TPR spectrograms of different Ni-Cu/SiO2 catalysts
2.7 催化剂活性评价
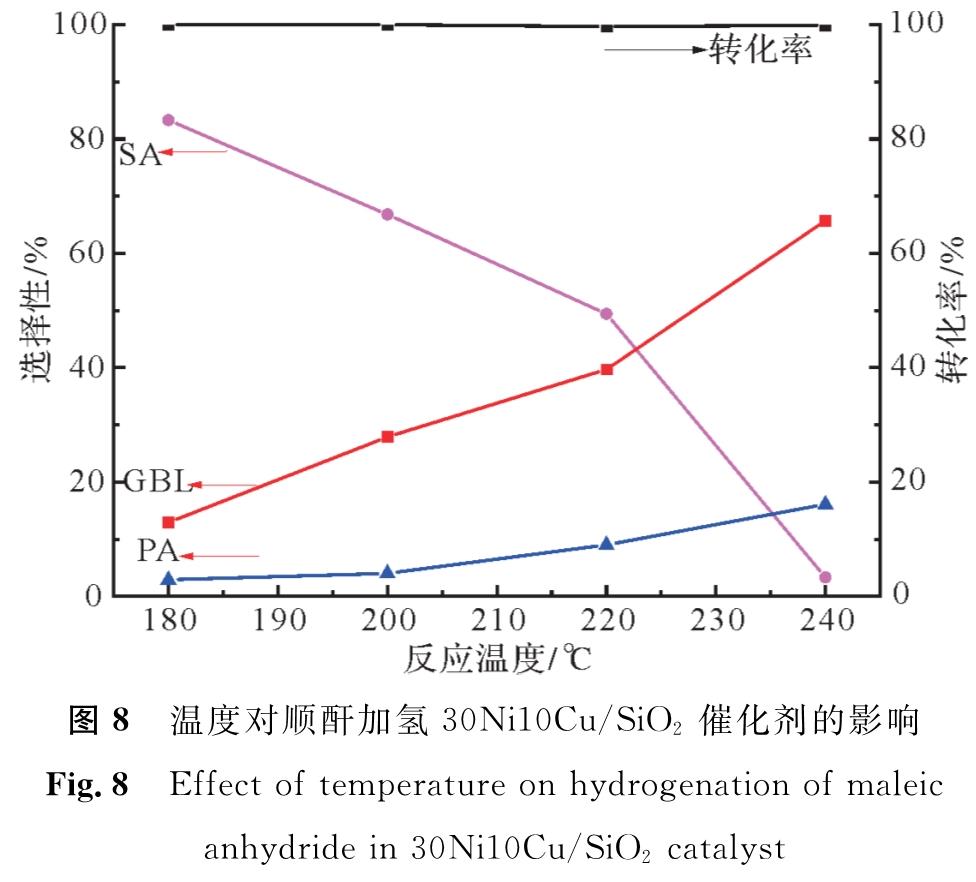
通过顺酐常压催化加氢反应来进行催化剂活性评价。使用30Ni10Cu/SiO2催化剂,在压力0.1 MPa、液体空速0.08 h-1和氢酐比78的条件下,考察反应温度对顺酐选择性加氢反应的影响,反应结果如图8所示,在180~240 ℃之间,顺酐加氢反应的转化率能达到99%以上,温度较低时,顺酐加氢主要产物是SA。随着温度的升高,SA的选择性下降,GBL的选择性逐渐上升,但副产物丙酸(propionic acid, PA)的选择性也升高,这是由于高温脱羰基所致。
图8 温度对顺酐加氢30Ni10Cu/SiO2催化剂的影响
Fig.8 Effect of temperature on hydrogenation of maleic anhydride in 30Ni10Cu/SiO2 catalyst
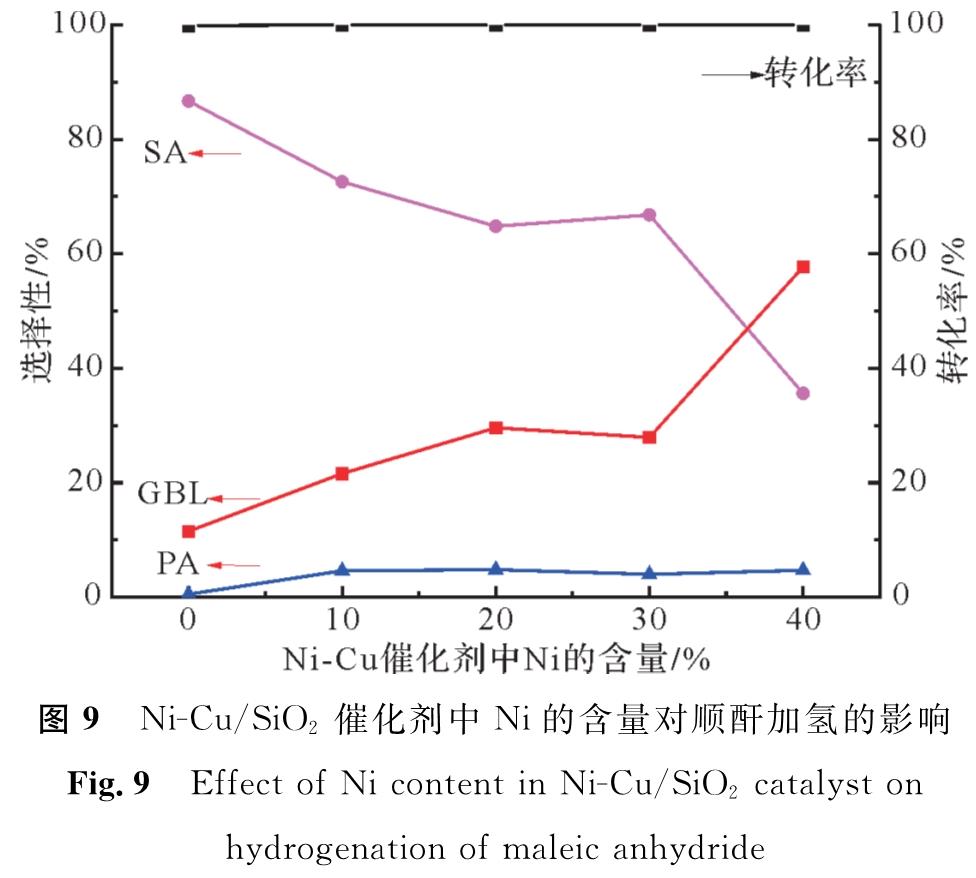
图9 Ni-Cu/SiO2催化剂中Ni的含量对顺酐加氢的影响
Fig.9 Effect of Ni content in Ni-Cu/SiO2 catalyst on hydrogenation of maleic anhydride
由于高温产生的丙酸会造成催化剂上活性组分流失,影响催化剂寿命。因此选择温度200 ℃,压力0.1 MPa,空速0.08 h-1,氢酐比78的条件下考察Ni-Cu/SiO2催化剂中Ni含量对顺酐加氢反应的影响,反应结果如图9所示,在200 ℃下,五种催化剂的转化率均能达到99%以上,随着Ni含量的增加,SA的选择性下降,GBL的选择性上升,但是副产物丙酸的选择性也随之上升。镍基催化剂在顺酐加氢反应中产生的丙酸普遍偏高,选择性达到4%以上,而铜基催化剂产生丙酸较低。丙酸主要由Ni基催化剂催化下SA氢解脱羰基而来[24]。
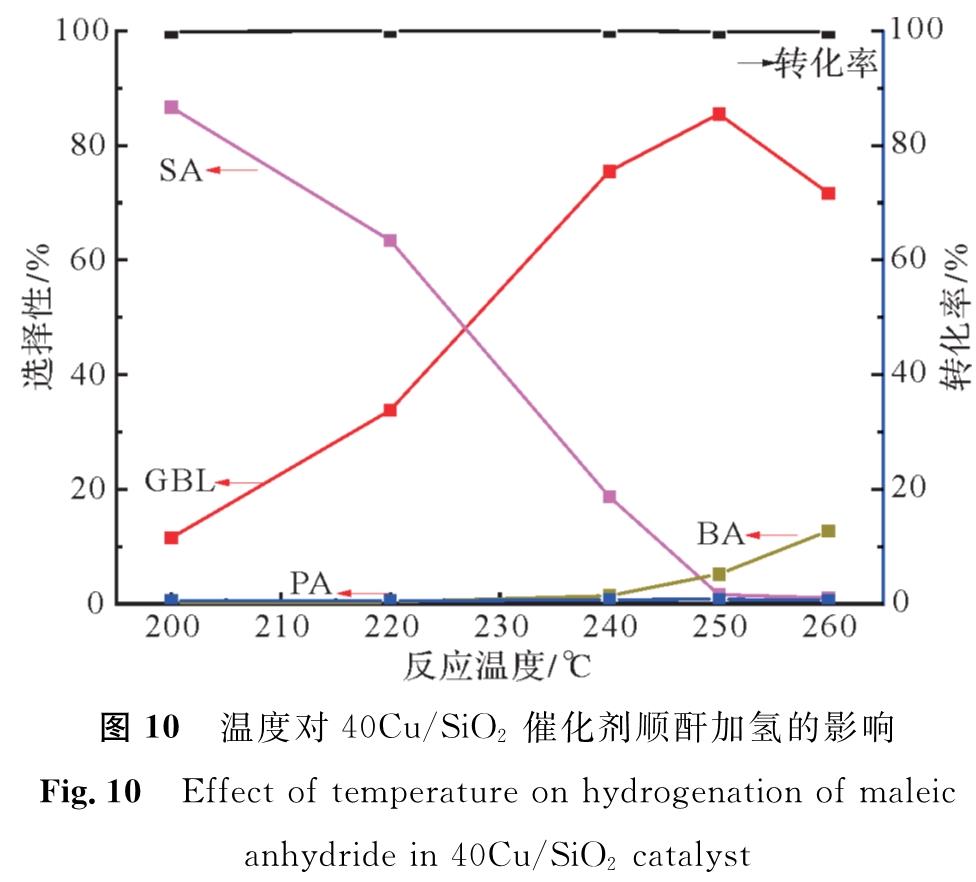
图 10 温度对40Cu/SiO2催化剂顺酐加氢的影响
Fig.10 Effect of temperature on hydrogenation of maleic anhydride in 40Cu/SiO2 catalyst
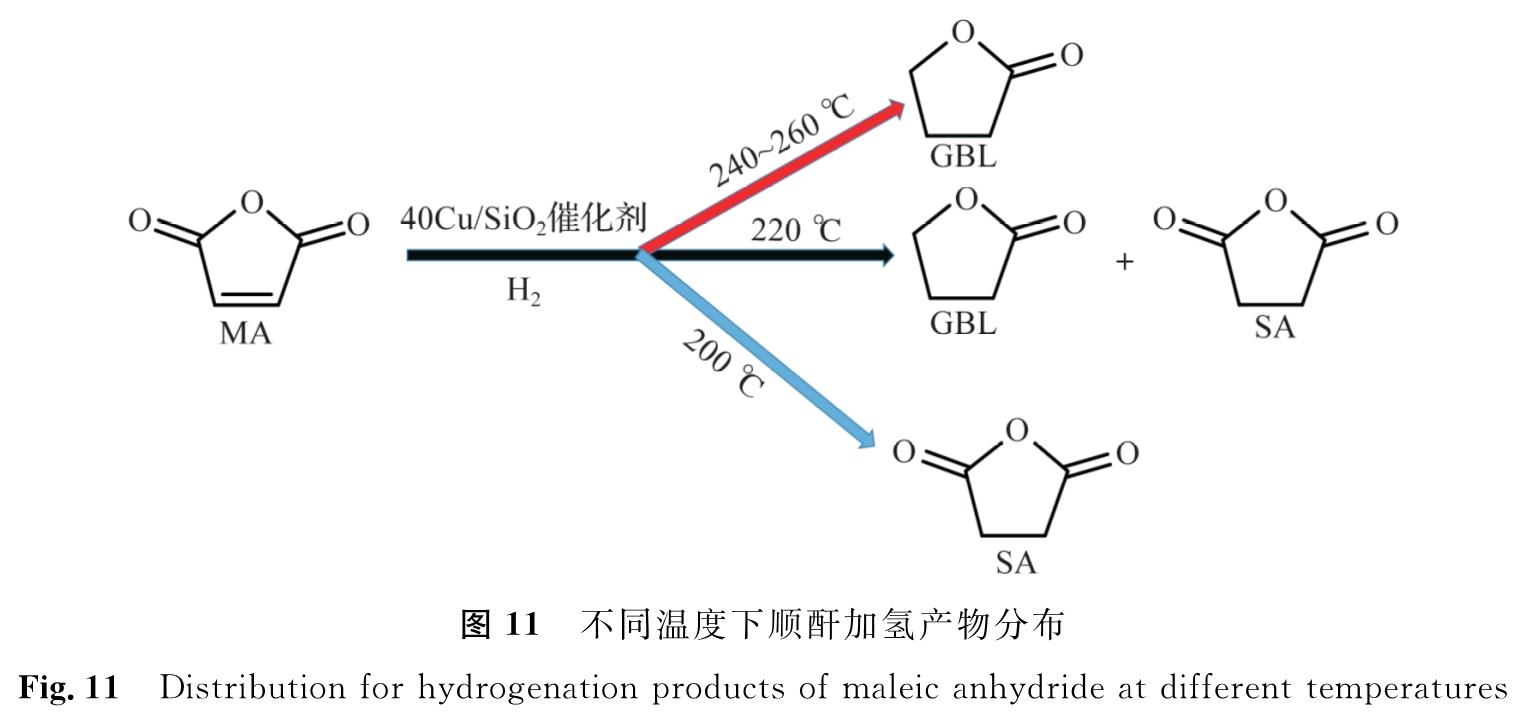
由于在常压顺酐加氢反应中镍基催化剂产生的副产物丙酸的选择性较高,会造成催化剂活性组分的流失,影响催化剂的活性和使用寿命,而铜基催化剂在顺酐加氢反应中丙酸等酸类副产物的含量低。因此,选择40Cu/SiO2催化剂在压力0.1 MPa、空速0.08 h-1和氢酐比78的条件下来考察温度对顺酐加氢反应的影响并测试其寿命。温度对40Cu/SiO2催化剂顺酐加氢的影响如图 10所示,在200~260 ℃之间,反应的转化率均能达到99%以上,SA的选择性随温度的上升而下降; GBL的选择性随着温度的上升而上升,在250 ℃时选择性最高达到85.1%,在260 ℃时GBL选择性下降。GBL选择性下降原因是GBL在高温下被过度加氢生成丁酸(butyric acid, BA)等其他副产物; 丙酸的选择性在200~260 ℃间均低于1%。240 ℃时GBL选择性为75.5%,SA选择性为18.7%,丙酸选择性为0.7%,丁酸选择性为1.4%,酸类副产物总选择性最低。较低的酸类副产物选择性可以减少催化剂活性组分的流失,延长催化剂使用寿命。因此,在240 ℃条件下更有利MA选择性加氢生成GBL。可见,反应温度是影响顺酐选择性加氢反应产物的主要因素,其不同温度下的产物分布如图 11所示,在200 ℃时其主要产物为SA,240~260 ℃时其主要产物为GBL,200~240 ℃产物则为SA和GBL。
图 11 不同温度下顺酐加氢产物分布
Fig.11 Distribution for hydrogenation products of maleic anhydride at different temperatures
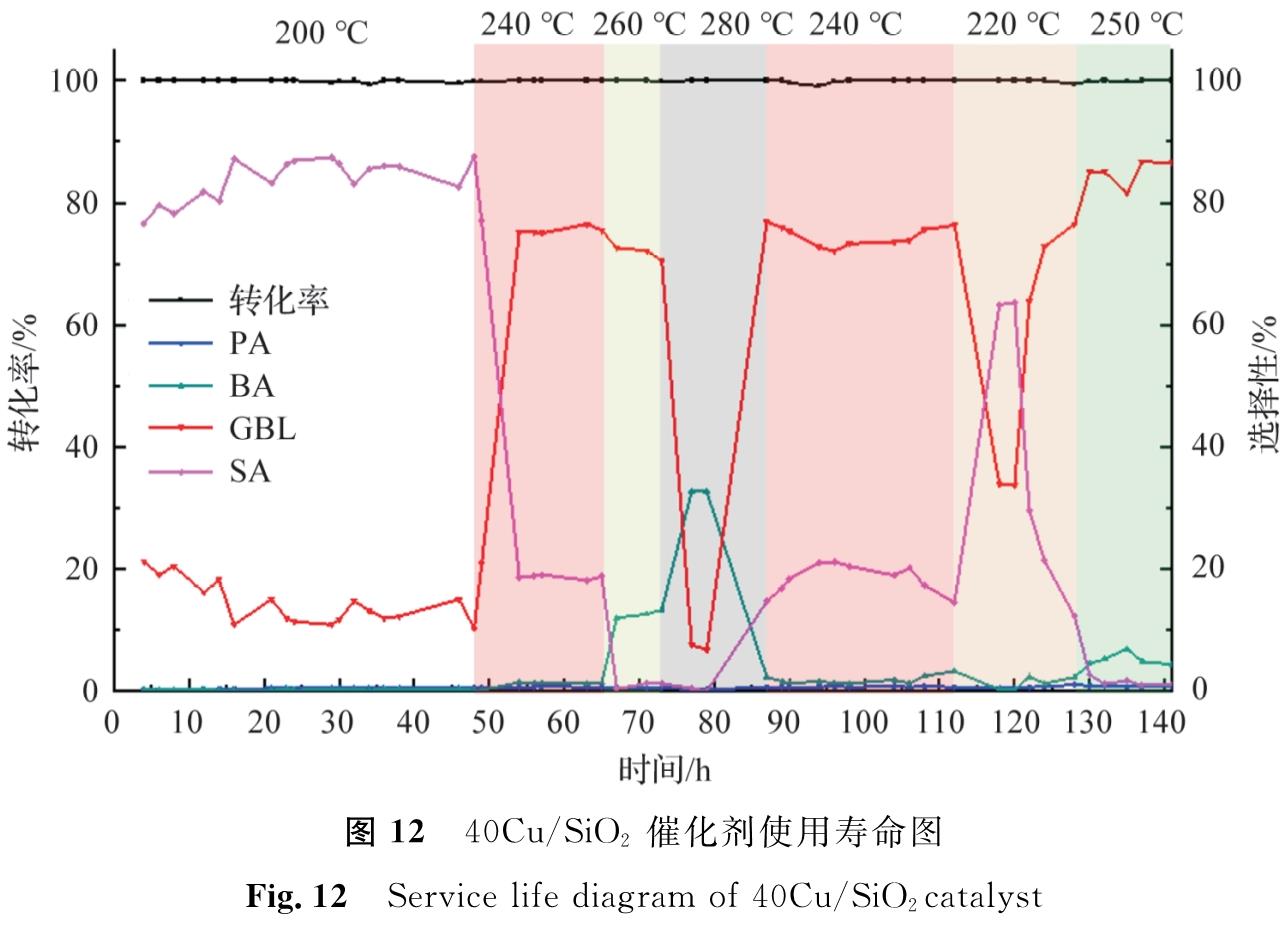
40Cu/SiO2催化剂使用寿命考察结果如图 12所示,在200~280 ℃之间,随着反应时间的增加,催化剂的MA转化率在140 h内没有明显降低,仍保持在99%以上,表现出优异的催化性能。
图 12 40Cu/SiO2催化剂使用寿命图
Fig.12 Service life diagram of 40Cu/SiO2catalyst
3 结 语
通过蒸氨法制备Ni-Cu/SiO2系列催化剂,研究了Ni-Cu双金属催化剂对催化顺酐选择性加氢产物分布的影响。Ni-Cu/SiO2系列催化剂都具有优异的顺酐加氢催化活性。结合XRD和XPS图谱可知,Ni、Cu双金属主要以页硅酸盐的形式存在,Ni0、Cu0和Cu+是其主要加氢活性位点。根据BET、H2-TPD和H2-TPR结果可知,Ni-Cu/SiO2催化剂都具有较大的比表面积,较强的氢气吸附能力。其中40Cu/SiO2的比表面积最大,孔径和孔体积最小,Cu粒子更分散,氢气吸附能力最强,更有利于GBL的生成。Ni、Cu含量和温度都是影响顺酐选择性加氢产物分布的主要因素,随着Ni含量的增加,Ni-Cu催化剂加氢能力也增强,但其强加氢能使得SA氢解为丙酸; 温度上升也会氢解SA和GBL,造成丙酸和丁酸升高,会降低催化剂的活性和寿命。因此,可以通过调节催化剂中的Ni、Cu含量和反应温度,来调节主要产物。筛选出了40Cu/SiO2催化剂用于顺酐选择性加氢生产GBL联产SA反应中,其GBL+SA选择性高、副产物少,寿命长。最佳温度为240 ℃,在此温度下GBL+SA选择性最高为94.2%,并且催化剂寿命长达140 h未见失活。本研究结果可为工业上规模化顺酐选择性加氢制备GBL联产SA提供参考。
- [1] ZHU J, DING X, LI D, et al. Graphene oxide-supported catalyst with thermoresponsive smart surface for selective hydrogenation of cinnamaldehyde[J]. ACS Applied Materials & Interfaces,2019,11(18):16443.
- [2] MURATA K, OGURA K, OHYAMA J, et al. Selective hydrogenation of cinnamaldehyde over the stepped and plane surface of Pd nanoparticles with controlled morphologies by CO chemisorption[J]. ACS Applied Materials & Interfaces,2020,12(23):26002.
- [3] STUCCHI M, MANZOLI M, BOSSOLA F, et al. Ruling factors in cinnamaldehyde hydrogenation:activity and selectivity of Pt-Mo catalysts[J]. Nanomaterials,2021,11(2):362.
- [4] ZHANG W, SHI W, JI W, et al. Microenvironment of MOF channel coordination with Pt NPs for selective hydrogenation of unsaturated aldehydes[J]. ACS Catalysis, 2020,10(10):5805.
- [5] YE H, ZHAO H, JIANG Y, et al. Catalytic transfer hydrogenation of the C=O bond in unsaturated aldehydes over Pt nanoparticles embedded in porous UiO-66 nanoparticles[J]. ACS Applied Nano Materials,2020,3(12):12260.
- [6] MAHATA N, CUNHA A F, ÓRFÃO J J M, et al. Highly selective hydrogenation of C=C double bond in unsaturated carbonyl compounds over NiC catalyst[J]. Chemical Engineering Journal,2012,188:155.
- [7] PRAKASH M G, MAHALAKSHMY R, KRISHNAMURTHY K R, et al. Studies on Ni-M(M = Cu, Ag, Au)bimetallic catalysts for selective hydrogenation of cinnamaldehyde[J]. Catalysis Today,2016,263:105.
- [8] JOSEPH ANTONY RAJ K, PRAKASH M G, ELANGOVAN T, et al. Selective hydrogenation of cinnamaldehyde over cobalt supported on alumina, silica and titania[J]. Catalysis Letters,2012,142(1):87.
- [9] DONG F, ZHU Y, ZHENG H, et al. Cr-free Cu-catalysts for the selective hydrogenation of biomass-derived furfural to 2-methylfuran:the synergistic effect of metal and acid sites[J]. Journal of Molecular Catalysis A:Chemical,2015,398:140.
- [10] 黄建兴,陈臣举,魏超,等.顺酐加氢合成1,4-丁二醇催化剂的研究进展[J].化学世界,2023,64(6):409.
- [11] 李太平,张涛,黄家兴,等.顺酐加氢制备γ -丁内酯催化剂研究进展[J].应用化工,2023,52(7):2192.
- [12] MEYER C I, REGENHARDT S A, BERTONE M E, et al. Gas-phase maleic anhydride hydrogenation over Ni/SiO2-Al2O3 catalysts:effect of metal loading[J]. Catalysis Letters,2013,143(10):1067.
- [13] 赵永祥,秦晓琴,武志刚,等.NiO-SiO2,NiO-Al2O3和NiO-Al2O3-SiO2催化剂上顺酐选择加氢性能的比较[J].燃料化学学报,2003(3):263.
- [14] 夏晓丽,谭静静,卫彩云,等.钼改性页硅酸镍催化剂催化顺酐加氢性能[J].高等学校化学学报,2019,40(6):1207.
- [15] 邱爱玲.顺酐加氢制γ -丁内酯Cu-CeO2-Al2O3催化剂失活与再生研究[J].能源化工,2015,36(3):4.
- [16] LIU M, YUAN L, FAN G, et al. NiCu nanoparticles for catalytic hydrogenation of biomass-derived carbonyl compounds[J]. ACS Applied Nano Materials,2020,3(9):9226.
- [17] BIAN Z, KAWI S. Highly carbon-resistant Ni-Co/SiO2 catalysts derived from phyllosilicates for dry reforming of methane[J]. Journal of CO2 Utilization,2017,18:345.
- [18] BAWAKED S, NARASIMHARAO K. Structural and catalytic properties of copper silicate nanomaterials[J]. Scientific Reports,2020,10(1):518.
- [19] GONG J, YUE H, ZHAO Y, et al. Synthesis of ethanol via syngas on Cu/SiO2 catalysts with balanced Cu0-Cu+ sites[J]. Journal of the American Chemical Society,2012,134(34):13922.
- [20] ZHOU S, KANG L, ZHOU X, et al. Pure acetylene semihydrogenation over Ni-Cu bimetallic catalysts:effect of the Cu/Ni ratio on catalytic performance[J]. Nanomaterials,2020,10(3):509.
- [21] PANG J, ZHENG M, WANG C, et al. Hierarchical echinus-like Cu-MFI catalysts for ethanol dehydrogenation[J]. ACS Catalysis,2020,10(22):13624.
- [22] DING J, POPA T, TANG J, et al. Highly selective and stable Cu/SiO2 catalysts prepared with a green method for hydrogenation of diethyl oxalate into ethylene glycol[J]. Applied Catalysis B:Environmental,2017,209:530.
- [23] DU H, MA X, JIANG M, et al. Efficient Ni/SiO2 catalyst derived from nickel phyllosilicate for xylose hydrogenation to xylitol[J]. Catalysis Today,2021,365:265.
- [24] MEYER C I, REGENHARDT S A, MARCHI A J, et al. Gas phase hydrogenation of maleic anhydride at low pressure over silica-supported cobalt and nickel catalysts[J]. Applied Catalysis A:General,2012,417/418:59.
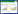 图 1 催化剂的XRD谱图
Fig.1 XRD profiles of catalysts
图 1 催化剂的XRD谱图
Fig.1 XRD profiles of catalysts